FDA concede la clearance 510(k) all'innovativa tecnologia di supporto cardiopolmonare di Abiomed
Comunicato Precedente

Comunicato Successivo

La Food and Drug Administration (FDA) statunitense ha concesso a Abiomed (NASDAQ: ABMD) una clearance 510(k) per un sistema di bypass cardiopolmonare compatto all-in-one chiamato Abiomed Breethe OXY-1 System™.
questo comunicato stampa include contenuti multimediali. Visualizzare l’intero comunicato qui: https://www.businesswire.com/news/home/20201026005788/it/
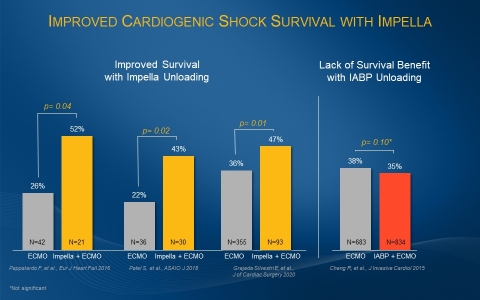
Figure 1 (Graphic: Business Wire)
Il sistema ECMO fornisce un supporto per il bypass cardiopolmonare ai pazienti i cui polmoni non sono più in grado di apportare una sufficiente ossigenazione dell'organo finale. La clearance 510(k) consiste nel pompare, ossigenare e rimuovere l'anidride carbonica dal sangue durante il bypass cardiopolmonare per un massimo di sei ore. Il sistema può aiutare a fornire ossigenazione ai pazienti che soffrono di shock cardiogeno o di insufficienza respiratoria come ARDS, H1N1, SARS o COVID-19.
Il testo originale del presente annuncio, redatto nella lingua di partenza, è la versione ufficiale che fa fede. Le traduzioni sono offerte unicamente per comodità del lettore e devono rinviare al testo in lingua originale, che è l'unico giuridicamente valido.
Vedi la versione originale su businesswire.com: https://www.businesswire.com/news/home/20201026005788/it/
Copyright Business Wire 2020Tom Langford
Director of Communication
(978) 882-8408
[email protected]
Permalink: http://www.businesswire.com/news/home/20201026005788/it/




