Lo studio clinico FAST dimostra elevata accuratezza diagnostica del software CAAS vFFR, che ha ricevuto dagli Stati Uniti l'autorizzazione alla commercializzazione FDA 510 (k)
(Photo: https://mma.prnewswire.com/media/693230/3D_Vessel.jpg )
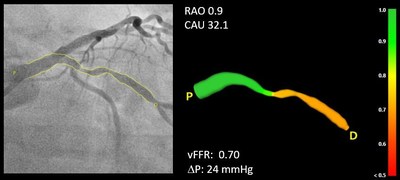
Il software - denominato CAAS vFFR (Cardiovascular Angiographic Analysis Systems for vessel Fractional Flow Reserve)-è in grado di calcolare la differenza di pressionecausata dalla presenza di una stenosi coronarica e i valori vFFR in modo non invasivo, evitando l'uso di guide di pressione dedicate o agenti iperemici.
La riserva frazionale di flusso, comunemente nota come FFR, rappresenta la metodica invasiva con maggiori evidenze scientifiche a supporto della sua utilità clinica per la valutazione funzionale delle stenosi coronariche. La FFR è il rapporto tra la pressione media a valle di una stenosi e la pressione media a monte della stessa durante iperemia massimale. Le informazioni ottenibili con l'indagine FFR, in molti contesti clinici ed angiografici, sono cruciali nella pianificazione di una procedura di angioplastica coronarica. L'esame viene eseguito utilizzando un catetere guida durante una procedura di cardiologia interventistica.
Il software CAAS vFFR consente ai medici cardiologi di utilizzare due immagini angiografiche acquisite nel corso di una normale procedura di cateterismo come input per eseguire una valutazione della fisiologia coronarica. Il CAAS vFFR consente una valutazione unica della lesione siadal punto di vista funzionale che anatomico, offrendoal cardiologo che esegue un intervento coronarico percutaneo ogni informazione per decidere il percorso migliore da intraprendere.
FAST, uno studio clinico condotto dal Dr. Ken Masdjedi e dal Dr. Joost Daemen dell'Erasmus Medical Center di Rotterdam, dimostra che il vFFR calcolato utilizzando CAAS vFFR ha un'alta correlazione lineare con la misurazione FFR eseguita per via invasiva.
"Nello studio FAST" ha commentato il Dr. Joost Daemen, responsabile dello studio clinico "abbiamo dimostrato che il vFFR calcolato utilizzando CAAS vFFR ha un'alta correlazione lineare con la misurazione FFR eseguita per via invasiva ed una elevata accuratezza diagnostica per rilevare un valore diFFR ≤ 0,80. Il vFFR è uno strumento promettente, veloce e facile da utilizzare per valutare la fisiologia coronarica, evitando la necessità di guide di pressione o di agenti iperemici costosi".
"Siamo molto orgogliosi di questo traguardo tecnologico e clinico", ha dichiarato René Guillaume, amministratore delegato di PMI, "che è il risultato dell'impegno e dell'esperienza trentennale della nostra azienda nel campo dello sviluppo di software dedicato all'analisi cardiovascolare e della collaborazione di successo con i più prestigiosi centri di ricerca scientifica e medica".
Il software CAAS vFFR ha ricevuto l'autorizzazione alla commercializzazione negli Stati Uniti (clearance 510 (k)), dall'Unione Europea (CE) e dal Giappone (PMDA).
Per ulteriori informazioni sul prodotto CAAS vFFR:
https://www.piemedicalimaging.com/product/caas-workstation/vffr/
PMI. PMI BV è leader mondiale nell'analisi quantitativa di immagini cardiovascolari, ben nota per il software CAAS e la linea di prodotti 3mensio. Con sede a Maastricht (Paesi Bassi), gestisce la vendita in tutto il mondo delle linee di prodotto CAAS e 3mensio. PMI e 3mensio Medical Imaging fanno parte del Gruppo Esaote, leader nel settore delle apparecchiature biomedicali, in particolare nei settori degli ultrasuoni, della risonanza magnetica dedicata e dell'Information Technology. Maggiori informazioni su PMI sono disponibili all'indirizzo www.piemedicalimaging.com
Per ulteriori informazioni si prega di contattare:
Ir. Tristan Slots
PMI T: +31-43-328-13-28
[email protected]
Mariangela Dellepiane
Esaote
+39-010-6547249
mob. +39-335-1289783
[email protected]





